腎機能や肝機能を低下させるリスクがある
4月7日、エボラ出血熱の点滴薬「レムデシビル」(商品名・ベクルリー)が新型コロナウイルス感染症の治療薬として日本で承認された。国内初の抗新型コロナウイルス薬となるが、厚労省は緊急時に審査する医薬品医療機器法の特例承認制度に沿って手続きを進め、その承認は申請後わずか3日と異例のスピードだった。通常、医薬品の承認は早くても申請から1年はかかる。
レムデシビルはアメリカの製薬会社ギリアド・サイエンシズがエボラ出血熱の治療薬として開発した医薬品だ。体内で新型コロナウイルスの増殖を抑える働きがあるとみられ、アメリカの臨床試験では患者の回復までの時間を3割ほど短縮する効果が確認された。ただ、日本の専門家からは「過度の期待はできない」との声もあがっている。
この薬をギリアド・サイエンシズ社は日本に無償で供給するというが、日本国内の医療機関に届く時期は、はっきりしていない。厚労省は重症の患者に優先的に投与するというが、問題は副作用である。腎機能や肝機能を低下させるリスクがあるのだ。
重症者向けのレムデシビル、軽症者向けのアビガン
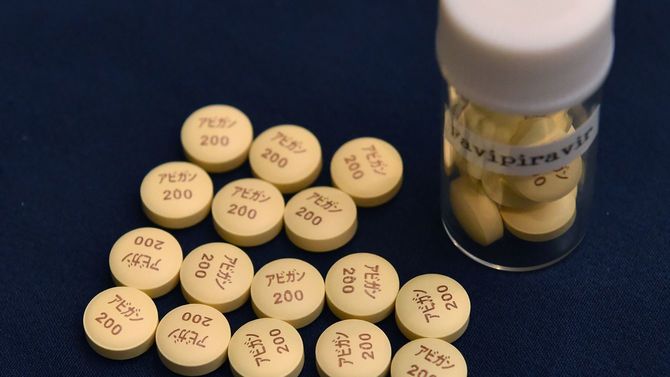
同じように新型コロナウイルスの増殖を抑える働きが期待されているのが、新型インフルエンザ治療薬の「アビガン」(一般名・ファビピラビル)である。
アビガンは富士フイルムの子会社富山化学が開発し、新型インフルエンザのため一定量が備蓄されている。レムデシビルと同様に既存の薬だが、用途が異なるために再承認が必要となる。既存薬は体内での働きが分かっているので、申請前の開発時間は短縮できる。
点滴するレムデシビルに比べ、アビガンは経口薬(飲み薬)で、医師や患者にとって使いやすい。アフリカではレムデシビルのようにエボラ出血熱の治療薬として使われ、それなりの効果が出ている。
安倍晋三首相が3月28日の記者会見で「これまでに患者の同意を得た臨床研究で数十例の投与が行われ、症状の改善に効果があった。今後は希望する国々と協力しながら臨床研究を拡大する」と発言して以来、注目されている。政府は重症者向けのレムデシビルに対し、アビガンは軽症者向けの治療薬として近く承認する方針だ。
安倍首相は4月7日の記者会見でもアビガンについて触れ、現在の備蓄量の3倍に相当する200万人分を準備することを明らかにしている。
しかしアビガンにも、深刻な副作用がある。胎児に奇形を起こす催奇形性だ。開発中のマウスに対する実験投与で奇形のマウスが生まれ、アフリカでは服用した男性の精液からアビガンの成分が検出されている。このため妊婦や子供をつくる予定のあるカップルには使用できない。
あらゆる医薬品は副作用のある「両刃の剣」である
レムデシビルやアビガン以外にも効果が期待される既存の薬はいくつかある。いずれも有効性と安全性をきちんとチェックして臨床現場で使う必要がある。新型コロナウイルス感染症に対する新薬やワクチンの開発も、急ぐ必要がある。
医薬品は副作用が避けられない。「両刃の剣」なのである。治療のどの過程でどう使うかなど、医療機関や臨床現場の医師らにはよく検討してもらいたい。患者に対するインフォームド・コンセント(十分な説明と同意)も欠かせない。こうした注意点は新薬やワクチンでも同じように重視しなければならない。
薬の副作用がもたらす「薬害」の歴史を私たちは知っている。
たとえば服用した妊婦から手足の短い子供が生まれた睡眠薬のサリドマイド、胃腸薬のキノホルムによって下半身の麻痺を引き起こしたスモン病、視力障害が問題にされた腎臓病治療薬のクロロキン、血友病の患者が血液製剤からエイズウイルスに感染した薬害エイズ事件、同じく血液製剤からは肝硬変や肝がんに進行するC型肝炎に感染する薬害も起きた。開頭手術のときの硬膜移植から感染が広まった薬害ヤコブ病も問題になった。薬害被害はいずれも甚大である。
なぜ薬害はなくならないのか。認可した厚生労働省は薬害の兆候があっても、認可した責任を問われたくないため、被害を小さくみた。製薬メーカーも患者の健康と命を預かっている責任を忘れ、目先の利益に走った。大学の教授や研究機関の研究者らは権威を保つために責任逃れを続けた。その結果、対応が遅れ、深刻な薬害被害が起きる。行政が何もしない不作為もあった。
新薬ですべてが解決するかの論調の産経社説
新型コロナウイルス感染症に既存薬を使うにせよ、新薬やワクチンを開発するにせよ、政府や医療機関は副作用や副反応を軽んじてはいけない。そもそもこれまで大半の患者が対処療法で治癒している。抗新型コロナウイルス薬の投与が本当に必要なのか。慎重に考えるべきだ。
「今の難局を乗り切るには治療薬やワクチンが不可欠である。各国の研究グループや製薬会社は新型コロナウイルスによる感染症を克服するため、治療薬やワクチンを用意しようと努めている」
「その先陣を切って米国発の治療薬『レムデシビル』が日本でも認可されたことを歓迎したい」
5月9日付の産経新聞の社説(主張)の書き出しである。「治療薬やワクチンが不可欠」とまで言い切るところや、「歓迎したい」との評価には驚かされる。見出しの「コロナ治療薬 アビガンも月内承認図れ」も書きすぎだ。新薬ですべてが解決するかの論調だ。薬害の歴史を無視してはいけない。
承認を急いだ結果、大惨事を起こした「イレッサ」
産経社説は続けて主張する。
「治療薬の候補は他にもある。日本の製薬会社が開発した抗インフルエンザ薬『アビガン』、ノーベル賞を受賞した大村智北里大特別栄誉教授が開発に貢献した抗寄生虫薬『イベルメクチン』、ぜんそくの治療薬『オルベスコ』などだ。医療の選択肢を拡大することは重要だ」
「米国の速度をみならうべきだ。安倍晋三首相がアビガンについて、5月中に新型ウイルスによる感染症治療薬としての薬事承認を目指していると表明した。臨床試験を迅速に進めてほしい」
候補が複数あって選択肢が広がることには沙鴎一歩も賛成である。しかし、「米国の速度をみならえ」との主張には反対だ。承認のスピードを上げた結果、惨事を起こした大きな薬害が起こした事例が日本にはあるからだ。
2002年7月、世界に先駆けて日本で承認された肺がん治療薬「イレッサ(一般名・ゲフィチニブ)」は劇的な効果がある一方で、承認後わずか半年でおよそ500人もの患者に間質性肺炎などを発症させ、うち約160人が亡くなった。イレッサの知識のない医師が処方したことが、多くの死者を出した原因だった。イレッサはその後、安全対策がとられ、患者の症状に合わせた的確な投与が行われている。薬の承認は早ければいいというわけにはいかないのである。
「現時点では全ての患者に効く特効薬とは言えない」
産経社説は後半で、「同時に、薬にはさまざまな副作用がある。効果と安全性に一定の留保がつくことは肝に銘じておくべきだ。使用に当たっては患者側への説明に努めてほしい」と書いている。副作用についてまったく触れていないわけではないが、読者の期待を煽るような書き方には問題がある。
毎日新聞の社説(5月9日付)は「新型コロナの治療薬 適切な使用で命守りたい」との見出しを付け、レムデシビルの問題点を整理している。
「まず、現時点では全ての患者に効く特効薬とは言えない」
「重症者約1000人を対象にした臨床試験では、回復までの時間を4日短縮できた。適切に使うことで人工呼吸器や集中治療室(ICU)に余裕が生まれ、医療崩壊防止につながると期待される」
「しかし、死亡率を下げる明確な効果は確認できなかった。米国製のため、日本でいつから使えるかや、必要な量が確保できるかも見通せない」
確かに「特効薬」ではないのだ。医療の崩壊を防げるメリットはあるが、これも確かなことではない。それにアメリカ製品ゆえの問題点も多い。
通常なら1年程度かかる審査を、わずか3日で済ませた
毎日社説は指摘する。
「安全性にも留意が必要だ。元々はエボラ出血熱の治療薬として開発中だった。米政府は非常事態を理由に新型コロナへの緊急使用を許可し、それを受けて日本も『特例承認』に踏み切った」
「病気のまん延防止に必要で、代替手段がなく、海外で認められているという要件を満たしたことから、通常なら1年程度かかる審査を、わずか3日で済ませた」
「一方で、副作用として肝臓や腎臓の機能障害が報告されている。リスクがあっても使用すべき有効性があるかどうか、細心の注意を払って症例を蓄積し、分析を続けるべきだ」
「安全性への留意」「リスクと有効性」など毎日社説は冷静にレムデシビルに言及している。読者として共感できる。薬剤は使う患者が多くなればなるほど、予想もしなかった新たな副作用が生まれる。毎日社説の主張のように「症例を集めて分析していく」ことが薬害を減らすことにつながる。



コメント